Accueil > Nos Actions > Journal de Bord des Opérations > Vacances Scientifiques > Au coeur du Vortex : cahier de labo
Introduction
L’aventure du Vortex continue cet été 2012 !
L’objectif de cette année est de fabriquer un prototype de petite taille afin de ne pas consommer trop d’eau au cours des tests et étalonnages. Ce prototype pourra être reproduit par les participants chez eux.
Le Journal de Bord
semaines du 08/07/12 au 22/07/12
Objectif : fabriquer un vortex de petite taille.
Réalisation :
![]() Rassembler le matériel
Rassembler le matériel
![]() Préparer les tubes, le support
Préparer les tubes, le support
![]() Assemblage
Assemblage
semaines du 22/07/12 au 05/08/12
Objectif :
![]() terminer le prototype du vortex
terminer le prototype du vortex
![]() faire quelques essais avec différentes solutions acides ou basiques
faire quelques essais avec différentes solutions acides ou basiques
Réalisation :
Schéma du Vortex :
Observations :
Le module filtreur de la session précédente est ici amélioré par des mesures de débit en ligne et par une amélioration de la distribution en eau. Il y a des fuites qui n’empêcheront pas les mesures. L’arrivée et la sortie des tuyaux pourront être améliorées grâce à un système d’embouts qui éviterait d’utiliser du mastique. Un robinet pourra être ajouté au tuyau d’évacuation.
Il faut réussir à caractériser le Vortex (débit, pression, température...) et continuer à tester son influence sur le pH de l’eau.
Essais avec différentes solutions acide et basiques :
![]() Formules :
Formules :
base forte : pH=14+log10(Cb).
base faible : pH=1/2(pKa+14+log10(Cb)).
mélange de solutions de pH connu :
pH=-log10(V1-10E-pH1+V2-10E-pH2/V1+V2).
pKa=constante propre à l’acide complémentaire de la base.
pH1, pH2, V1, V2=Ph et volume des solutions 1 et 2
![]() Espèces retenues :
Espèces retenues :
hydroxyde de sodium MMNaOH=40g/mol ; Solubilité=1090 g/L.
levure chimique : hydrogénocarbonate de sodium + pyrophosphate de sodium : MMNaHCO3-= 84g/mol ; Solubilité=87g/L ; MMNa4P2O7= 266g/mol ; Solubilité=6g/100mL.
ammoniac MMNH3= 17g/mol ; Solubilité=540g/L.
acétate d’éthyle MMC4H8O2= 62g/mol ; Solubilité=83g/L.
![]() Mode opératoire : Faire passer dans le vortex 25 L de solution de NaOH d’une part et de Levure chimique d’autre part. Effectuer 6 Passages avec la solution sortant par les côtés.
Mode opératoire : Faire passer dans le vortex 25 L de solution de NaOH d’une part et de Levure chimique d’autre part. Effectuer 6 Passages avec la solution sortant par les côtés.
Mesurer le pH avant le passage dans le vortex.
Prise d’échantillon (1 tube à essai) à chaque passage de la solution de sortie côtés et centrale et mesure de pH.
Témoin négatif (sans passage dans le vortex) : mesurer le pH dans la cuve d’entrée au cours de l’expérimentation et en fin d’expérimentation.
Manipuler avec blouse, gants, lunettes et bottes.
![]() Résultats :
Résultats :
![]() Remarques :
Remarques :
Attacher les tuyaux de sortie côtés ensemble pour le recueil dans un seau.
Concentration de soude trop élevée ! Il faut la diluer pour avoir pH=9.
Interprétation :
![]() Calcul des forces centrifuges :
Calcul des forces centrifuges :
Formule : Fc=mw2r.
m=masse de la particule en kg.
w=vitesse radicale en rad/s ; w= v/r.
r= distance entre le centre et le centre de gravité des particules (norme en m).
v= vitesse en m/s.
D= débit en m/s ; D=v/s.
s= section du tuyau en m2.
r= rayon du cercle (centre à centre de la particule) en m.
Fc=m.v/r.r=m.D/sr.r=m.D/s.
![]() Données :
Données :
D=2,78.10E-7x350=9,73.10E-5m3/s.
s=5,024.10E-7m2.
D/s=1.93.10E2m/s.
![]() Masses atomiques :
Masses atomiques :
sodium/ion Na+ : 22,98u = 3,9.10E-25 kg.
oxygène : 16u = 3,07.10E-26 kg.
carbone : 12u = 1,92.10E-26 kg.
hydrogène : 1u = 1,6.10E-27 kg.
ion hydrogénocarbonate HCO3- : 3.15u+12u+1u=61u=9,76.10E-26 kg.
ion hydroxyde OH- : 16u+1u=17u= 2,72.10E-26 kg.
Phosphore : 30,97u= 4,9.10E-26 kg.
ion pyrophosphate P2O7 4- : 2.30,97u+7.12u= 143,94u= 2,3.10E-24 kg.
![]() Forces centrifuges :
Forces centrifuges :
Fc(HCO3-)= 9,76.10E-26.1,93.10E2= 1,88.10E-23N.
Fc(P2O7 4-)= 2,30.10E-24.1,93.10E2= 4,4.10E-22N.
Fc(Na+)= 3,9.10E-26.1,93.10E2= 1,06.10E-23N.
Fc(OH-)= 2,72.10E-26.1,93.10E2= 5,25.10E-24N.
Conclusions : Force extrêmement faible exercée sur les particules (de 10E-24 à 10E-22N).
![]() Interprétation :
Interprétation :
L’ion pyrophosphate P2O7 4- est le plus entraîné vers les parois du vortex.
L’ion Hydroxyde OH- a le plus tendance à rester au centre.
Levure chimique : en théorie, les ions P2O7 2- migrent vers l’extérieur, les ions HCO3- et Na+ restent au centre.
Donc le pH des sorties côté devrait augmenter alors que celui de la sortie du centre devrait être inchangé ou augmenter moins.
Nos résultats montrent une augmentation des pH de sortie côtés et centrale avec une augmentation plus rapide en sortie centrale.
Il y a bien un effet du vortex sur le pH mais la séparation des ions HCO3- dans le vortex n’est pas flagrante.
Il est possible que les ions Na+ soient captés par des ions Cl- de l’eau du robinet pour former du sel.
Soude : en théorie, les ions Na+ migrent vers l’extérieur, les ions OH- restent au centre car ils sont très petits.
Donc le pH des sorties côté devrait être stable ou diminuer alors que celui de la sortie du centre devrait augmenter beaucoup.
Nos résultats montrent une augmentation importante des pH de sortie côtés et centrale avec une augmentation plus rapide en sortie centrale.
Il y a bien un effet du vortex sur le pH mais la séparation des ions OH- dans le vortex n’est pas flagrante. l’ion Na+ a peut-être été déplacé vers l’extérieur.
Remèdes :
![]() Pompe plus puissante car la vitesse à l’entrée du vortex est insuffisante. Le vortex devra être dans ce cas conçu dans un matériau plus solide.
Pompe plus puissante car la vitesse à l’entrée du vortex est insuffisante. Le vortex devra être dans ce cas conçu dans un matériau plus solide.
![]() Revoir les dimensions du vortex, les molécules n’ont peut-être pas le temps de se réorganiser avant la sortie du vortex. Dans ce cas, il faudrait un vortex plus long mais on peut aussi augmenter le diamètre du vortex pour différencier davantage l’éloignement du centre des molécules.
Revoir les dimensions du vortex, les molécules n’ont peut-être pas le temps de se réorganiser avant la sortie du vortex. Dans ce cas, il faudrait un vortex plus long mais on peut aussi augmenter le diamètre du vortex pour différencier davantage l’éloignement du centre des molécules.
![]() Un tube transparent permettrait de vérifier l’initiation correcte du vortex.
Un tube transparent permettrait de vérifier l’initiation correcte du vortex.
![]() L’eau du robinet induit des réactions chimiques parasites(les ions Cl- captent les ions Na+ et les ions K+ captent les ions OH-). Il faudrait utiliser de l’eau distillée pour ces manipes mais les quantités requises sont trop élevées.
L’eau du robinet induit des réactions chimiques parasites(les ions Cl- captent les ions Na+ et les ions K+ captent les ions OH-). Il faudrait utiliser de l’eau distillée pour ces manipes mais les quantités requises sont trop élevées.
![]() Conclusions : Le Vortex a une action immédiate sur les solutions testées mais la séparation des ions n’est pas nette. Il faudrait tester avec de l’eau distillée et des pressions plus importantes.
Conclusions : Le Vortex a une action immédiate sur les solutions testées mais la séparation des ions n’est pas nette. Il faudrait tester avec de l’eau distillée et des pressions plus importantes.
A long terme, il faudrait essayer un vortex avec le cône inférieur inversé et une pression plus élevée afin d’initier une inversion du cyclone produit. Le 1er cyclone descendant (primaire) retient les grosses molécules, et le cyclone inversé (secondaire), passant à l’intérieur du cyclone primaire, remonte les plus petites particules vers la sortie du haut.
A court terme, nous pouvons mesurer l’effet du vortex sur de grosses particules comme l’argile et mesurer l’effet du gradient de pression formé par le vortex en travaillant sur des solutions salines à saturation.
Enfin, nous devons améliorer le vortex en essayant de combler les fuites et l’esthétique avec un nouveau système d’arrivée et de sortie d’eau. Il faut aussi un bouchon pour la sortie du haut.
semaines du 05/08/12 au 12/08/12
Défi séparation : Panoramix se fait vieux, il a oublié la formule de sa célèbre potion magique ! La seule solution, est d’en séparer tous les constituants... Dites à Panoramix le nombre et la nature des constituants de sa potion.
![]() composition de la potion magique :
composition de la potion magique :
10 c à soupe de sel, 10 cl d’huile, 5 c à soupe de limaille de fer, copeaux de liège, sable ou terre dans 1 L d’eau du robinet.
![]() matériel :
matériel :
1 cuve pour accueillir la potion magique.
Béchers plastiques.
Spatules.
Passoire.
Coton.
Filtres à café.
Barquettes en plastique pour recueillir les différents constituants.
Sopalin.
Ampoule de décantation (pas pour une solution terreuse ou sableuse ! Ca la bouche).
Réchaud et casserole.
Aimants.
Conductimètre.
![]() principes de séparation :
principes de séparation :
L’écumage permet de séparer le surnageant : liège.
Le grillage ou la décantation (passoire permet de séparer les gros constituants (sable ou terre, limaille de fer).
La limaille de fer peut être séparée du sable avec un aimant.
L’ampoule à décantation permet de séparer l’huile et un culot de particules plus petites.
La filtration (filtres à café ou coton) permet de séparer les particules restantes de terre non dissoutes mais restant dans la phase acqueuse. Attention, l’huile colmate les filtres ! Il faut l’éliminer avant de filtrer.
On vérifie la différence de salinité avec notre solution obtenue et l’eau pour voir s’il y a des substances dissoutes avec le conductimètre.
L’ébullition permet de séparer les substances dissoutes (sel).
![]() penser à faire des essais avec de petits échantillons.
penser à faire des essais avec de petits échantillons.
![]() Passation : disposer la potion magique et le matériel nécessaire sur une table et lancer le défit. : « avec le matériel qui est sur la table, il faut réussir à séparer et identifier les 6 constituants de la potion magique de Panoramix ». Il faut coopérer et repenser à ce que vous savez sur les méthode de purification.
Passation : disposer la potion magique et le matériel nécessaire sur une table et lancer le défit. : « avec le matériel qui est sur la table, il faut réussir à séparer et identifier les 6 constituants de la potion magique de Panoramix ». Il faut coopérer et repenser à ce que vous savez sur les méthode de purification.

- Décantation de la « potion » sans le surnageant
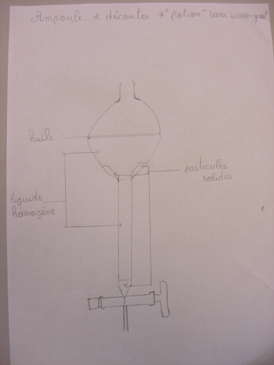
- Schéma de l’ampoule à décanter
1ers tests avec l’argile verte surfine.
![]() Théorie : les particules d’argile devraient être rejetées à l’extérieur du tourbillon. Nous attendons une concentration de la solution aux sorties extérieures et une dilution de la solution en sortie centrale.
Théorie : les particules d’argile devraient être rejetées à l’extérieur du tourbillon. Nous attendons une concentration de la solution aux sorties extérieures et une dilution de la solution en sortie centrale.
![]() Mode opératoire : 30 g d’argile dans 25 L d’eau du robinet
Mode opératoire : 30 g d’argile dans 25 L d’eau du robinet
et 3 g d’argile dans 25 L d’eau du robinet.
Effectuer les passages dans le vortex en recyclant l’eau qui sort par les côtés.
Prendre un échantillon avant Vortex.
Prendre 6 échantillons sorties côtés.
Prendre 6 échantillons sortie centrale.
Observer le trouble dans chaque tube à l’oeil nu. Laisser décanter 1 nuit et observer le culot.
![]() Résultats : Le trouble est identique dans tous les tubes, avant et après vortex. Il n’y a aucune différence notoire entre les deux sorties.
Résultats : Le trouble est identique dans tous les tubes, avant et après vortex. Il n’y a aucune différence notoire entre les deux sorties.
Les culots sont aussi identiques.
![]() Conclusion : l’argile n’est pas envoyé vers les bords du vortex.
Conclusion : l’argile n’est pas envoyé vers les bords du vortex.
![]() remèdes : des tests peuvent être fait avec des pains d’argile de qualité différente.
remèdes : des tests peuvent être fait avec des pains d’argile de qualité différente.
2e tests avec la spiruline.
![]() Théorie : La spiruline est une algue bleue riche en protéines et en fer. elle peut servir de colorant alimentaire. Les particules de spiruline devraient être rejetées à l’extérieur du tourbillon. Nous attendons une concentration de la solution aux sorties extérieures et une dilution de la solution en sortie centrale.
Théorie : La spiruline est une algue bleue riche en protéines et en fer. elle peut servir de colorant alimentaire. Les particules de spiruline devraient être rejetées à l’extérieur du tourbillon. Nous attendons une concentration de la solution aux sorties extérieures et une dilution de la solution en sortie centrale.
![]() Mode opératoire : 7,5 g de spiruline dans 25 L d’eau du robinet
Mode opératoire : 7,5 g de spiruline dans 25 L d’eau du robinet
et 3 g de spiruline dans 25 L d’eau du robinet.
Effectuer les passages dans le vortex en recyclant l’eau qui sort par les côtés.
Prendre un échantillon avant Vortex.
Prendre 6 échantillons sorties côtés.
Prendre 6 échantillons sortie centrale.
Observer la coloration dans chaque tube à l’oeil nu. Laisser décanter 1 nuit et observer le culot.
![]() Résultats : Avant le passage dans le vortex, la solution présente des agrégats fins de spiruline sans aucun trouble. Après vortex, la solution devient trouble et les agrégats ont disparus. Le trouble est identique dans tous les tubes, après vortex. Il n’y a aucune différence notoire entre les deux sorties.
Résultats : Avant le passage dans le vortex, la solution présente des agrégats fins de spiruline sans aucun trouble. Après vortex, la solution devient trouble et les agrégats ont disparus. Le trouble est identique dans tous les tubes, après vortex. Il n’y a aucune différence notoire entre les deux sorties.
Après décantation, les culots sont plus petits après vortex qu’avant vortex et ont même disparus pour 3 g de spiruline.
![]() Interprétation : la spiruline a pu précipité sous la pression induite dans le vortex. Le tourbillon a aussi pu simplement mélangé les agrégats.
Interprétation : la spiruline a pu précipité sous la pression induite dans le vortex. Le tourbillon a aussi pu simplement mélangé les agrégats.
![]() Conclusion : la spiruline n’est pas envoyée vers les bords du vortex. En revanche le vortex a une action sur la spiruline encore ininterprétée.
Conclusion : la spiruline n’est pas envoyée vers les bords du vortex. En revanche le vortex a une action sur la spiruline encore ininterprétée.
![]() Remèdes : nous pouvons essayer d’agiter une même solution de spiruline pour voir si l’on obtient le même effet que le vortex.
Remèdes : nous pouvons essayer d’agiter une même solution de spiruline pour voir si l’on obtient le même effet que le vortex.
![]() L’expérience a été refaite avec 5 et 10 g de spiruline dans 25 L d’eau avec un témoin négatif (agitation de la solution dans un tube à essai à la main durant le temps de l’expérience) et un témoin positif (vortex de la solution induite par un agitateur magnétique durant le temps de l’expérience).
L’expérience a été refaite avec 5 et 10 g de spiruline dans 25 L d’eau avec un témoin négatif (agitation de la solution dans un tube à essai à la main durant le temps de l’expérience) et un témoin positif (vortex de la solution induite par un agitateur magnétique durant le temps de l’expérience).
Les deux témoins présentent un trouble identique à celui observé après passage dans le vortex.
Après décantation, le culot bleu est plus petit qu’avant passage dans le vortex mais plus gros qu’après passage dans le vortex.
En revanche le culot de précipité blanc n’est pas présent. Nous avons donc bien un effet propre au vortex sur la spiruline.
Les résultats des tests correspondent à ceux trouvés pour 3 et 7,5 g de spiruline (voir tableau).
Il semble donc que le trouble soit dû au vortex et pas à une simple agitation.








